古德帕斯彻综合征是一种自身免疫综合征,涉及由循环抗肾小球基底膜抗体引起的肺泡性肺出血和肾小球肾炎。古德帕斯彻综合征最常发生在具有遗传易感性和吸烟的个体中,但碳氢化合物吸入和病毒性呼吸道感染也可能是其他因素。古德帕斯彻综合征的症状包括呼吸困难、咳嗽、疲劳、咯血和/或血尿。对于出现咯血或血尿的患者,应怀疑患有古德帕斯彻综合征,并通过血液中存在抗肾小球基底膜抗体来确诊。古德帕斯彻综合征的治疗包括血浆置换、糖皮质激素和免疫抑制剂(例如环磷酰胺)。如果在出现呼吸衰竭或肾衰竭之前开始治疗,则预后良好。
古德帕斯彻综合征 (Goodpasture's syndrome) 最初由古德帕斯彻 (Goodpasture) 于 1919 年描述。古德帕斯彻综合征是指在存在抗肾小球基底膜 (GBM) 抗体的情况下,同时出现肾小球肾炎和肺泡出血的疾病。古德帕斯彻综合征最常表现为弥漫性肺泡出血和肾小球肾炎的合并症,但有时也会导致单独的肾小球肾炎 (10-20%) 或肺部受累 (10%)。男性发病率高于女性。
什么原因导致古德帕斯彻综合征?
该病的病因尚未完全明确。目前推测该病与古德帕斯彻综合征的遗传易感性有关,其标记物被认为是HLA-DRW2基因。有观点认为,既往病毒感染(甲型肝炎病毒和其他病毒性疾病)、工业危害和药物(主要是D-青霉胺)可能起着一定作用。
肺出血肾炎综合征(Goodpasture's syndrome)的发病机制是肾脏和肺泡的肾小球毛细血管基底膜自身抗体的形成。这些抗体属于IgG类,在补体C3成分存在的情况下,它们与基底膜抗体结合,随后引发肾脏和肺泡的免疫性炎症。
抗肾小球基底膜 (GBM) 抗体针对的是 IV 型胶原 3 链的非胶原 (NC-1) 结构域,该结构域在肾和肺毛细血管的基底膜中浓度最高。环境因素(吸烟、病毒性急性呼吸道感染 (ARI) 和吸入碳酸氢盐悬浮液(较常见))以及肺炎(较少见)会激活具有遗传易感性人群(通常是 HLA-DRwl5、-DR4 和 -DRB1 等位基因携带者)的肺泡毛细血管抗原向循环抗体的呈递。循环抗肾小球基底膜抗体与基底膜结合,固定补体,并诱导细胞炎症反应,导致肾小球肾炎和/或肺毛细血管炎的发生。
肾脏和肺泡的肾小球毛细血管基底膜自身抗原可能存在一定的共性。自身抗原是在病因损伤作用的影响下形成的。未知的病因会损伤并改变肾脏和肺的基底膜结构。当肾小球基底膜受损时,其降解产物的排泄速度减慢甚至减少,这自然为肾脏和肺发生自身免疫性损伤创造了条件。目前尚不完全清楚基底膜的哪种成分会成为自身抗原。目前推测是肾脏肾小球基底膜的内部结构成分——4型胶原蛋白的α3链。
形成的免疫复合物沉积在肾小球毛细血管的基底膜上,导致肾小球(肾小球肾炎)和肺泡(肺泡炎)中发生免疫炎症过程。参与这种免疫炎症发展的主要细胞是T淋巴细胞、单核细胞、内皮细胞、多形核白细胞和肺泡巨噬细胞。它们之间的相互作用由分子介质、细胞因子(生长因子 - 血小板、胰岛素样生长因子、β-转化生长因子、白细胞介素-1、肿瘤坏死因子等)介导。花生四烯酸代谢物、自由基、蛋白水解酶和粘附分子在免疫炎症的发展中起着重要作用。
肺泡巨噬细胞的激活在古德帕斯彻综合征的肺泡炎发展中至关重要。在激活状态下,它们会分泌约40种细胞因子。第一类细胞因子(趋化因子、白三烯、白细胞介素-8)可促进多形核白细胞向肺部流动。第二类细胞因子(生长因子 - 血小板、巨噬细胞)可促进成纤维细胞向肺部移动。肺泡巨噬细胞还会产生活性氧,即蛋白酶,这些酶会损伤肺组织。
古德帕斯彻综合征的病理形态学
Goodpasture综合征的主要病理形态学表现为:
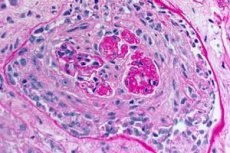
- 主要损害肾脏和肺的微循环床。肺部可观察到静脉炎、小动脉炎和毛细血管炎的征象,并伴有明显的破坏和增生现象;毛细血管损害主要见于肺泡间隔,并发生肺泡炎,肺泡内有出血性渗出物。肾脏损害的特征是发生毛细血管外增生性肾小球肾炎,随后形成玻璃样变性和纤维化,最终导致肾衰竭;
- 明显的肺泡内出血;
- 由于肺泡炎的发展,导致不同程度的肺含铁血黄素沉着症和肺硬化症。
古德帕斯彻综合征的症状
该疾病最常见的临床表现是肺部病变。咯血是最显著的症状;然而,在出现出血表现时,也可能没有咯血,患者可能仅表现为胸部X线片上的浸润性改变,或伴有浸润征兆和呼吸窘迫和/或衰竭。呼吸困难(主要伴有劳力)、咳嗽、不适、工作能力下降、胸痛、发热和体重下降很常见。高达40%的患者有肉眼血尿,尽管肺出血可能在肾脏表现出现前数周至数年出现。
咯血期间,呼吸困难可能会加剧。虚弱和工作能力下降也值得关注。
肺出血肾炎综合征的症状随时间变化,肺部听诊音从清晰到湿啰音不等。部分患者因贫血而出现外周水肿和苍白。
检查时应注意皮肤苍白、黏膜发绀、面部苍白或明显肿胀、肌力下降、体重下降。体温通常升高至发热水平。
当叩击肺部时,可能会在广泛的肺出血灶上发现叩击音缩短,但这种情况很少见;更常见的是,叩击音没有变化。
肺出血肾炎综合征的特征性听诊体征是干湿喘息,在咯血期间或之后,干湿喘息的次数会显著增加。
心血管系统检查可发现动脉高血压,可能出现左侧相对心浊音界增大、心音低沉、收缩期杂音及心包摩擦音,并伴有严重肾衰竭。在严重动脉高血压的背景下,肾脏损害逐渐加重,可能出现急性左心室衰竭,并伴有心源性哮喘和肺水肿。通常,这种情况发生在疾病的终末期。
肾脏损害通常在肺部症状出现后一段时间才会显现。肾脏病变的特征性临床症状包括血尿(有时为肉眼可见血尿)、快速进展的肾衰竭、少尿和动脉高血压。
在10-15%的病例中,Goodpasture综合征始于肾脏病理的临床症状 - 出现肾小球肾炎的临床表现(少尿,水肿,动脉高血压,明显苍白),然后出现肺损伤的症状。许多患者可能患有肌痛,关节痛。
无论起病形式如何,Goodpasture综合征在大多数情况下病情严重,病情持续进展,并导致严重的肺功能和肾功能衰竭。患者发病后预期寿命为数月至1-3年不等。患者通常死于尿毒症或肺出血。
古德帕斯彻综合征的诊断
诊断Goodpasture综合征需要通过间接免疫荧光法检测血清抗肾小球基底膜(GBM)抗体,或(如条件允许)使用重组人NC-1α3进行直接酶联免疫吸附试验(ELISA)。其他血清学检测,例如抗核抗体(ANA)检测,可用于检测系统性红斑狼疮(SLE),抗链球菌溶血素O滴度检测可用于诊断链球菌感染后肾小球肾炎,而链球菌感染后肾小球肾炎可能是许多肺肾综合征病例的病因。25%的Goodpasture综合征病例的ANCA抗体呈阳性(在外周标本中)。如果存在肾小球肾炎(血尿、蛋白尿、尿液分析中发现红细胞泥和/或肾衰竭),则可能需要进行肾活检。在Goodpasture综合征和所有其他原因引起的肺肾综合征患者中,肾活检结果显示为进展性局灶节段性坏死性肾小球肾炎。肾脏或肺组织的免疫荧光染色通常显示IgG沿肾小球或肺泡毛细血管呈线性沉积。糖尿病肾病和纤维性肾小球肾炎(一种罕见的导致肺肾综合征的疾病)也可见这种沉积,但这些疾病中GBM抗体的检测并不具有特异性。
肺功能检查和支气管肺泡灌洗无法确诊肺出血肾炎综合征,但可用于确诊患有肾小球肾炎和肺部浸润但无咯血的患者是否存在弥漫性肺泡出血。多次冲洗后,如果灌洗液仍呈出血性,则可能确诊弥漫性出血综合征,尤其是在伴有血细胞比容下降的情况下。
 [ 3 ]
[ 3 ]
古德帕斯彻综合征的实验室诊断
- 常规血液分析。特征性表现为缺铁性低色素性贫血、低色素性贫血、红细胞大小不均、红细胞异形性。还可见白细胞增多、白细胞数左移以及血沉显著增快。
- 尿液常规分析。尿液中可检出蛋白质(蛋白尿程度可显著)、圆柱状(颗粒状、透明状、红细胞状)、红细胞(可出现肉眼血尿)。随着慢性肾衰竭的进展,尿液相对密度降低,在齐姆尼茨基试验中可出现等密度低尿。
- 生化血液检查。血液中尿素、肌酐、结合珠蛋白、血清粘蛋白、a2 和 γ 球蛋白含量升高,铁含量降低。
- 免疫学检查。可检测到T淋巴细胞抑制因子数量减少,并可检测到循环免疫复合物。通过间接免疫荧光或放射免疫学方法检测肾小球和肺泡毛细血管基底膜抗体。
- 痰液分析。痰液中含有大量红细胞,可检测到含铁血黄素和噬铁细胞。
古德帕斯彻综合征的仪器诊断
- 肺部X光检查。特征性X光征象为肺根部浸润影,并扩散至肺下部和中部,以及进行性、对称性、双侧云状浸润影。
- 研究外部呼吸功能。肺量计检查显示患者为限制性呼吸衰竭(肺活量下降),随着病情进展,患者会出现阻塞性呼吸衰竭(FEV1下降,蒂芬诺指数下降)。
- 心电图。可见贫血和缺氧导致的严重心肌营养不良征象(多个导联T波振幅和ST段间期缩短,最常见于左胸导联)。严重动脉高血压患者可出现左心室心肌肥厚的征象。
- 血气分析显示动脉低氧血症。
- 肺和肾活检。如果无法通过非侵入性方法准确诊断,则需要进行肺组织活检(开放活检)和肾脏活检,以最终确诊。活检样本需进行组织学和免疫学检查。以下体征是古德帕斯彻综合征的特征:
- 存在肾小球肾炎(最常见的是毛细血管外)、出血性肺泡炎、含铁血黄素沉着症和间质纤维化的形态学体征;
- 采用免疫荧光法检测肺泡和肾小球基底膜上IgG 和补体成分 C3的线性沉积。
古德帕斯彻综合征的诊断标准
在诊断 Goodpasture 综合征时,建议使用以下标准。
- 肺部病变和肾脏病变的结合,即咯血(常有肺出血)、呼吸急促和肾小球肾炎症状。
- 随着呼吸和肾衰竭的发展,疾病进程稳步进展。
- 缺铁性贫血的发展。
- 在肺部 X 光检查过程中发现,在肺部图案网状变形的背景下,存在多个双侧云状浸润。
- 检测血液中针对肾小球和肺泡基底膜的高滴度循环抗体。
- 检测肾小球和肺泡毛细血管基底膜上的 IgG 和补体成分 C3 的线性沉积。
- 没有其他全身性表现(肺和肾除外)。
Goodpasture综合征的鉴别诊断
Goodpasture综合征必须与多种以咯血或肺出血为表现的疾病相鉴别。需排除支气管和肺部肿瘤性疾病、结核病、肺脓肿、支气管扩张、心血管疾病(导致肺循环充血和高血压)、系统性血管炎和出血性素质。
古德帕斯彻综合征筛查项目
- 一般血液和尿液检查。
- 生化血液测试:测定总蛋白和蛋白质部分、肌酐和尿素、转氨酶、血清粘蛋白、结合珠蛋白、纤维蛋白、铁。
- 痰液分析:细胞学检查、噬铁细胞测定。
- 免疫学研究:测定B淋巴细胞和T淋巴细胞、T淋巴细胞亚群、免疫球蛋白、循环免疫复合物、肾脏和肺泡肾小球基底膜抗体的含量。
- 肺部X光检查。
- 心电图。
- 肺量测定。
- 肺和肾活检检查。
古德帕斯彻综合征的治疗
肺出血肾炎综合征的治疗包括每日或隔日进行血浆置换,共计 2 至 3 周(4 L 血浆置换)以清除抗肾小球基底膜抗体,同时联合静脉注射糖皮质激素(通常为甲基强的松龙 1 g,至少 20 分钟,隔日 3 次,泼尼松龙 1 mg/kg 体重,每日一次)和环磷酰胺(2 mg/kg,每日一次),共计 6 至 12 个月,以防止新抗体的形成。当肺功能和肾功能不再改善时,可以减少治疗。长期死亡率与疾病发作时的肾功能损害程度有关;早期需要透析的患者和活检显示新月体肾单位超过 50% 的患者生存期不到 2 年,除非考虑肾移植,否则通常需要透析。咯血可能是一个很好的预后指标,因为它可以及早发现疾病;少数ANCA阳性患者对古德帕斯丘综合征的治疗反应较好。少数病例会出现复发,这与持续吸烟和呼吸道感染有关。对于接受肾移植的终末期肾病患者,肾移植后疾病可能复发。
古德帕斯彻综合征的预后如何?
古德帕斯彻综合征通常进展迅速,除非及时诊断和治疗,否则可能致命;如果在出现呼吸衰竭或肾衰竭之前开始治疗,则预后良好。
肺出血和呼吸衰竭时的立即存活与确保气道通畅有关;对于动脉血气水平处于临界值且即将发生呼吸衰竭的患者,建议进行气管插管和机械通气。


