心脏瓣膜
最近審查:04.07.2025
心脏瓣膜是如何排列的?
对瓣膜血液供应的研究始于 N. Luschka (1852),他向心脏血管注射了造影剂。他发现主动脉和肺动脉的房室瓣和半月瓣的瓣尖内有许多血管。同时,许多病理解剖学和组织学手册指出,未改变的人类心脏瓣膜不含血管,而后者仅在各种病理过程中才会出现在瓣膜中 - 各种病因的动脉粥样硬化和心内膜炎。关于血管缺失的信息主要基于组织学研究。人们假设,由于瓣尖的游离部分没有血管,它们的营养是通过从冲洗瓣尖的血浆中过滤液体来实现的。人们注意到有少量血管与横纹肌组织纤维一起渗入瓣膜基部和腱索。
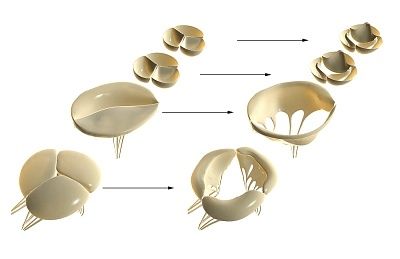
然而,当向心脏血管中注入各种染料(明胶印度墨水、明胶铋、黑色印度墨水水悬液、胭脂红或台盼蓝溶液)时,发现血管会随着心肌组织穿透房室心脏瓣膜、主动脉瓣膜和肺动脉,稍稍不能到达瓣膜的游离缘。
在房室瓣瓣尖的疏松纤维结缔组织中,发现个别主血管与心脏横纹肌组织邻近区域的血管吻合。
最多的血管位于瓣膜基部,而位于瓣膜游离部分的血管数量相对较少。
根据K.I. Kulchitsky等人(1990)的研究,二尖瓣的动脉和静脉血管直径较大。该瓣膜瓣尖的底部主要分布着主血管,其细环状毛细血管网延伸至瓣尖底部,占瓣尖面积的10%。三尖瓣的动脉血管直径小于二尖瓣。该瓣膜瓣尖主要分布着分散的血管和相对较宽的毛细血管环。二尖瓣的前瓣血供更集中,而三尖瓣的前瓣和后瓣则起着主要的关闭功能。成年人心脏房室瓣的动脉血管与静脉血管直径之比为1:1.5。毛细血管袢呈多边形,垂直于瓣膜瓣尖底部。这些血管在心房侧内皮下形成平面网络。血管也存在于腱索中,它们从左右心室的乳头肌穿透而出,距离可达腱索长度的 30%。许多血管在腱索底部形成弓形袢。主动脉和肺动脉干的心脏瓣膜在血液供应方面与房室瓣有显著不同。直径相对较小的主血管接近主动脉和肺动脉干瓣膜的半月瓣底部。这些血管的短分支终止于不规则的椭圆形和多边形毛细血管袢。它们主要位于半月瓣底部附近。主动脉瓣和肺动脉瓣底部的静脉血管直径也小于房室瓣底部的静脉血管直径。成年人心脏主动脉瓣和肺动脉瓣的动脉血管和静脉血管直径之比为1:1.4。短侧支从较大的血管延伸出来,末端形成不规则椭圆形和多边形的毛细血管环。

随着年龄增长,结缔组织纤维(包括胶原纤维和弹性纤维)会变粗,疏松纤维状未成形结缔组织的数量会减少,房室瓣瓣叶以及主动脉瓣和肺动脉瓣的半月瓣叶组织会逐渐硬化。瓣膜内心脏横纹肌纤维的长度会缩短,因此其数量和穿过心脏瓣膜的血管数量也会减少。由于这些变化,心脏瓣膜会失去其弹性和回弹性,从而影响瓣膜的关闭机制和血流动力学。
心脏瓣膜具有毛细淋巴管网络和少量配有瓣膜的淋巴管。瓣叶的毛细淋巴管具有特征性外观:其管腔非常不均匀,不同区域的同一条毛细淋巴管的直径不同。在几条毛细淋巴管汇合的地方,会形成扩张 - 各种形状的腔隙。淋巴管网的襻通常呈不规则的多边形,较少见的是椭圆形或圆形。淋巴管网的襻通常不闭合,毛细淋巴管的末端是盲目的。淋巴管襻通常沿着从瓣叶游离缘到其基部的方向延伸。在某些情况下,在房室瓣的瓣叶中会发现双层毛细淋巴管网。
心内膜神经丛位于其各层,主要位于内皮下。在瓣叶的游离缘,神经纤维主要呈放射状分布,与腱索连接。靠近瓣叶基底部,形成一个网状神经丛,与纤维环周围的神经丛连接。在半月瓣叶,心内膜神经网络较为稀疏。在瓣膜附着处,神经网络变得致密且多层。
心脏瓣膜的细胞结构
瓣膜间质细胞负责维持瓣膜的结构,其形状细长,具有众多延伸至整个瓣膜基质的细小突起。瓣膜间质细胞有两种形态和结构上的差异:一种具有收缩特性,其特征是存在收缩原纤维;另一种具有分泌特性,具有发达的内质网和高尔基体。收缩功能可抵抗血流动力学压力,并通过心脏和骨骼收缩蛋白的产生进一步支持,这些收缩蛋白包括 α 和 β 肌球蛋白的重链以及各种肌钙蛋白亚型。已证实心脏瓣叶收缩是多种血管活性药物的反应,这表明协调的生物刺激对于瓣膜功能的成功发挥至关重要。
间质细胞也是心脏瓣膜等结构修复系统的重要组成部分。瓣叶的持续运动及其伴随的结缔组织变形会造成损伤,而瓣膜间质细胞会做出反应,以维持瓣膜的完整性。修复过程似乎对正常的瓣膜功能至关重要,而目前人工瓣膜模型中这些细胞的缺失可能是导致生物瓣膜结构损伤的一个因素。
间质细胞的一个重要研究领域是研究它们与周围基质之间由黏着斑分子介导的相互作用。黏着斑是特殊的细胞-基质相互作用位点,通过整合素将细胞骨架与基质蛋白连接起来。它们也充当信号转导位点,传递来自细胞外基质的机械信息,从而引发包括但不限于细胞黏附、迁移、生长和分化等反应。了解瓣膜间质细胞的细胞生物学特性,对于阐明这些细胞之间以及与周围环境相互作用的机制至关重要,这样才能在人工瓣膜中重现这一功能。
为开发心脏瓣膜这一颇具前景的组织工程方向,间质细胞研究正运用多种技术开展。细胞骨架的存在可通过对波形蛋白、结蛋白、肌钙蛋白、α-肌动蛋白和平滑肌肌球蛋白、α-和β-肌球蛋白重链、心肌肌球蛋白轻链-2、α-和β-微管蛋白进行染色来确认。细胞收缩性可通过对肾上腺素、血管紧张素Ⅱ、缓激肽、卡巴胆碱、氯化钾、内皮素Ⅰ的阳性反应来确认。细胞间的相互关系可通过功能性间隙相互作用来确定,并通过羧基荧光素微注射进行验证。基质分泌可通过对脯氨酰-4-羟化酶/Ⅱ型胶原、纤连蛋白、硫酸软骨素和层粘连蛋白进行染色来确认。神经支配由运动神经末梢的紧密分布决定,这反映在神经肽Y酪氨酸羟化酶、乙酰胆碱酯酶、血管活性肠肽、P物质、辣椒素基因相关肽的活性上。促有丝分裂因子由血小板衍生的生长因子、碱性成纤维细胞生长因子和5-羟色胺(5-HT)评估。所研究的间质细胞成纤维细胞的特征是基底膜不完整,胞质突起细长,与基质紧密连接,内质网和高尔基体发育良好,微丝丰富,并形成粘附键。
瓣膜心内膜细胞在每个心脏瓣膜周围形成一个功能性的血栓形成鞘,类似于血管内皮。广泛使用的瓣膜置换方法消除了心内膜的保护功能,这可能导致血小板和纤维蛋白在人工瓣膜上沉积,引起细菌感染和组织钙化。这些细胞的另一个可能功能是调节下面的瓣膜间质细胞,类似于内皮对平滑肌细胞的调节。内皮和邻近细胞之间存在复杂的相互作用,部分由内皮细胞分泌的可溶性因子介导。这些细胞在管腔侧形成一个巨大的表面,上面覆盖着微突起,从而增加了与循环血液中代谢物质的暴露以及可能的相互作用。
内皮细胞常常由于血流对血管壁产生的剪切应力而表现出形态和功能的差异,这也适用于瓣膜心内膜细胞,其呈现细长或多边形形状。细胞结构的变化可能是由于局部血液动力学对细胞骨架成分的作用或由底层细胞外基质变化引起的继发效应引起的。在超微结构水平上,瓣膜心内膜细胞具有细胞间连接、浆囊泡、粗面内质网和高尔基体。虽然它们在体内和体外都能产生血管性血友病因子,但它们缺乏韦伯-帕拉德小体(含有血管性血友病因子的特定颗粒),而韦伯-帕拉德小体是血管内皮细胞的特征性细胞器。瓣膜心内膜细胞的特点是连接牢固、功能性间隙相互作用和重叠的边缘褶皱。
心内膜细胞即使在体外也保留其代谢活性:它们产生血管性血友病因子、前列环素、一氧化氮合酶,具有血管紧张素转换酶活性,并大量分泌粘附分子ICAM-1和ELAM-1,这些分子在免疫反应发展过程中对于结合单核细胞至关重要。在利用组织工程技术构建人工瓣膜的理想细胞培养物时,应考虑所有这些指标,但瓣膜心内膜细胞本身的免疫刺激潜力可能会限制其应用。
心脏瓣膜的细胞外基质由纤维状胶原蛋白、弹性蛋白大分子、蛋白聚糖和糖蛋白组成。胶原蛋白占瓣膜干重的60%,弹性蛋白占10%,蛋白聚糖占20%。胶原蛋白成分为瓣膜提供主要的机械稳定性,其代表类型为I型(74%)、II型(24%)和V型(2%)。胶原蛋白丝束被弹性蛋白鞘包裹,弹性蛋白鞘介导胶原蛋白丝之间的相互作用。蛋白聚糖分子的糖胺聚糖侧链倾向于形成凝胶状物质,其他基质分子在其中相互作用形成永久键,其他成分沉积。人体心脏瓣膜的糖胺聚糖主要由透明质酸组成,其次是硫酸皮肤素、4-硫酸软骨素和6-硫酸软骨素,以及少量的硫酸肝素。基质组织的重塑和更新受基质金属蛋白酶 (MMP) 及其组织抑制剂 (TI) 调控。这些分子还参与更广泛的生理和病理过程。一些金属蛋白酶,包括间质胶原酶 (MMP-1、MMP-13) 和明胶酶 (MMP-2、MMP-9) 及其组织抑制剂 (TI-1、TI-2、TI-3),存在于所有心脏瓣膜中。金属蛋白酶的过量产生是心脏瓣膜病理状态的特征。
 [ 6 ], [ 7 ], [ 8 ], [ 9 ], [ 10 ], [ 11 ], [ 12 ], [ 13 ], [ 14 ], [ 15 ], [ 16 ]
[ 6 ], [ 7 ], [ 8 ], [ 9 ], [ 10 ], [ 11 ], [ 12 ], [ 13 ], [ 14 ], [ 15 ], [ 16 ]
心脏瓣膜及其形态结构
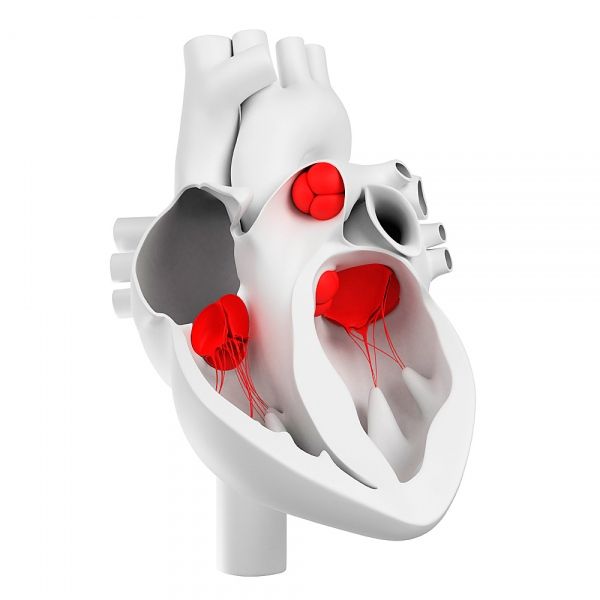
心脏瓣膜由三层形态不同且功能重要的瓣叶基质组成:纤维层、海绵层和心室层。
纤维层由多层胶原纤维构成,构成瓣叶的抗负荷框架。这些纤维呈放射状排列,形成褶皱,使动脉瓣在关闭时能够伸展。纤维层位于这些瓣膜的出口外表面附近。房室瓣的纤维层是腱索胶原束的延续。它位于海绵层(入口层)和心室层(出口层)之间。
纤维层和心室层之间是海绵层(海绵质层)。海绵层由组织松散的结缔组织和粘稠的介质组成。该层的主要基质成分是蛋白多糖,由随机排列的胶原蛋白和薄层弹性蛋白组成。蛋白多糖分子的侧链带有强负电荷,这影响了其与水的结合能力,并形成了多孔的基质凝胶。基质的海绵层可以减轻心脏瓣膜瓣叶的机械应力,并保持其柔韧性。
心室层比其他层薄得多,富含弹性纤维,使组织能够抵抗持续的变形。弹性蛋白具有海绵状结构,包裹并连接胶原纤维,使胶原纤维保持中性折叠状态。瓣膜的入口层(动脉瓣膜为心室层,房室瓣膜为海绵层)比出口层含有更多的弹性蛋白,这可以减轻瓣尖闭合时产生的液压冲击。胶原蛋白和弹性蛋白之间的这种关系使瓣尖能够拉伸高达40%,而不会发生稳定变形。当承受较小负荷时,该层的胶原蛋白结构会朝向负荷方向,从而增强其对进一步负荷增长的抵抗力。
因此,将心脏瓣膜视为简单的心内膜重复的想法不仅过于简化,而且本质上是错误的。心脏瓣膜是复杂的器官,包含横纹肌纤维、血管和淋巴管以及神经成分。无论其结构还是功能,瓣膜都是所有心脏结构不可或缺的一部分。对正常瓣膜功能的分析必须考虑其细胞组织,以及细胞间以及细胞与基质之间的相互作用。从这些研究中获得的知识对于利用组织工程设计和开发瓣膜假体具有重要意义。


