多巴胺
最近審查:03.07.2025
適應症 多巴胺
多巴胺的使用指征包括维持慢性心力衰竭、创伤、肾衰竭,甚至开胸手术和心肌梗死或脓毒症休克患者的血压。低剂量 DA 给药也可用于治疗低血压、低心输出量和器官衰竭(通常以低尿量为指征)。在 Horniewicz 的实验表明帕金森病患者的尾状核中 DA 减少后,DA 在中枢神经系统 (CNS) 中获得了重要的临床重要性。此外,静脉注射其氨基酸前体 L-DOPA(L-二羟基苯丙氨酸)可减轻帕金森病症状。[ 3 ] 由于血脑屏障阻止 DA 从体循环进入中枢神经系统,因此 DA 对帕金森病等中枢神经系统疾病无效。然而,L-DOPA 可以成功穿过血脑屏障,可以全身给药,包括口服片剂。虽然治疗性多巴胺替代疗法可有效缓解运动症状,但它可能导致运动副作用和成瘾相关的行为问题(例如,冲动控制障碍)[ 4 ],[ 5 ],[ 6 ]
發布表單
多巴胺以浓缩液形式存在于安瓿瓶中,用于输液。
藥效學
多巴胺生物合成遵循与去甲肾上腺素 (NE) 相同的酶促序列。事实上,DA 是 NE 合成的前体(见图)。[ 7 ],[ 8 ] DA 合成的第一步是限速反应,涉及酪氨酸羟化酶 (TH) 将 L-酪氨酸转化为 L-多巴 (L-DOPA)。[ 9 ],[ 10 ] 该转化需要氧气、铁辅因子和四氢生物蝶呤 (BH4 或 THB),导致羟基添加到芳香环上形成 L-多巴。随后,该分子在芳香族 L-氨基酸脱羧酶的作用下转化为 DA,并去除羧基。DA 合成后,通过囊泡单胺转运体 2 (VMAT2) 转运到突触囊泡,再到达突触末梢。[ 11 ],[ 12 ]
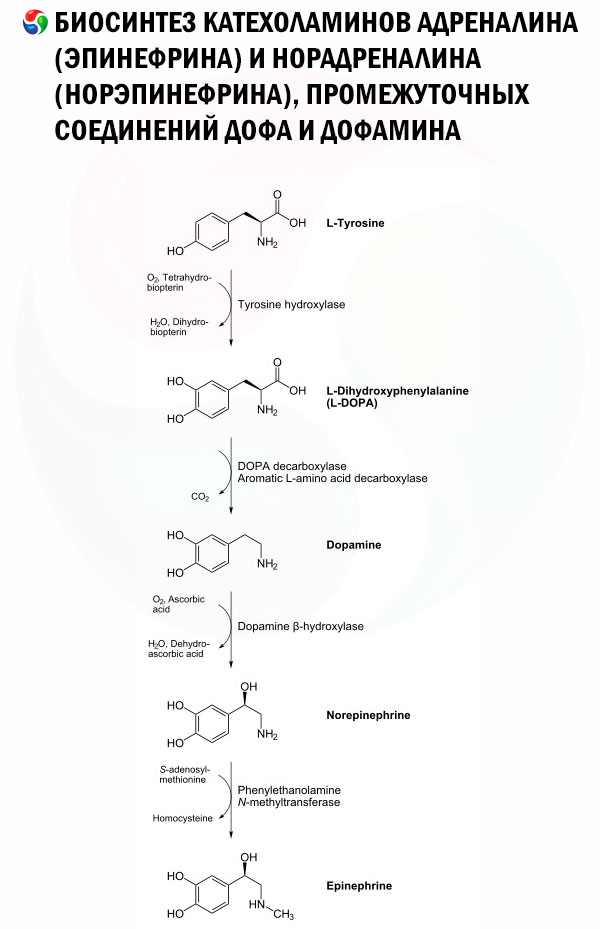
如果一个人经常大量摄入L-酪氨酸,它会像左旋多巴一样轻易穿过血脑屏障。[ 13 ] 但由于多巴胺(DA)无法穿过血脑屏障,其作用在空间上受到限制。然而,如果L-酪氨酸水平较低,L-苯丙氨酸可以通过苯丙氨酸羟化酶转化为L-酪氨酸。
多巴胺(DA)释放到突触空间后,会与突触前和突触后末梢上的各种受体相互作用,从而引起目标神经元的兴奋或抑制。DA受体分为两大家族,包含五种不同的亚型,每种亚型分别影响不同的细胞内信号通路。[ 14 ] 多巴胺受体家族D1和D2根据定义都是G蛋白偶联受体,但D1受体会导致神经元去极化,而D2受体则抑制神经元兴奋。[ 15 ]
一旦进入突触间隙,DA就会通过DA转运蛋白(DAT)转运回突触前神经元进行重新包装,或者可能留在细胞外空间,被神经胶质细胞摄取或经细胞膜代谢。DA可以在神经元外通过儿茶酚-O-甲基转移酶(COMT)代谢为3-甲氧基酪胺(3-MT),而单胺氧化酶-B(MAO-B)会快速将3-MT代谢为高香草酸(HVA)。[ 16 ]此外,DA也可以在细胞质内代谢,在MAO-A和醛脱氢酶(ALDH)的双重作用下,DA会转化为酚酸3,4-二羟基苯乙酸(DOPAC)。[ 17 ]
鉴于这一复杂的过程,多巴胺调节可以在多个层面发生,例如整个神经元、其投射或神经系统的神经回路。此外,在DA合成(转录、翻译和翻译后调控)、突触体包装(VMAT调节、囊泡运输至突触)、DA释放(神经元去极化、钙信号传导、囊泡融合)以及通过调节相应酶及其相对于底物的空间定位而进行的再摄取和代谢过程中,也起着调节作用。[ 18 ]
如前所述,DA 的系统作用依赖于各种受体(D1、D2、D3、D4 和 D5)以及 α 和 β 肾上腺素能受体。这些 G 偶联受体通常被归类为 D1 或 D2,这主要基于其传统的生化功能,表明多巴胺可以调节腺苷酸环化酶活性。[ 19 ] 然而,根据其分子结构、生化特性和药理作用,DA 受体进一步分为 D1 类(D1 和 D5)或 D2 类(D2、D3、D4)。[ 20 ],[ 21 ]
平滑肌、近端肾小管和皮质集合管上的D1受体激活会增加利尿。[ 22 ] D2受体位于肾神经、肾小球和肾上腺皮质的突触前。这些神经的激活会导致肾脏钠和水的排泄减少。[ 23 ] 阿扑吗啡是一种DA受体激动剂,可能对这些DA受体有类似的激活作用。[ 24 ] 肾上腺素能受体也能与DA结合,增强动脉平滑肌收缩和心脏窦房结传导,从而解释其对心脏的治疗作用。
尽管血脑屏障特别限制了DA从体循环向中枢神经系统的转移,但进一步研究发现,DA在寻求奖赏行为中起着核心作用,在这种行为中,DA的转移显著增加。目前对DA的研究包括表观遗传学改变及其与多种精神疾病的关系,包括药物滥用和成瘾、精神分裂症和注意力缺陷障碍。[ 25 ],[ 26 ] 总的来说,这些疾病与中脑边缘和中脑皮质DA通路的紊乱有关。成瘾药物对中枢神经系统的一个常见影响是纹状体DA释放增加,这通常与高运动活动和刻板行为有关。 [ 27 ] 纹状体中 DA 的增加是由于来自黑质致密部 (SN) 和腹侧被盖区 (VTA) 的轴突投射所致,这些轴突投射到伏隔核和杏仁核。[ 28 ],[ 29 ]
另一个 DA 回路,即结节漏斗通路,主要负责调节来自垂体前叶的神经内分泌催乳素,该激素以诱导泌乳而闻名,但在水盐稳态、免疫反应和细胞周期调节中也起次要作用。[ 30 ],[ 31 ] 黑质纹状体通路是与帕金森病中观察到的运动缺陷有关的主要通路。[ 32 ] 该通路涉及起源于黑质(致密部)的多巴胺能神经元,并通过内侧前脑束投射到纹状体,分别与壳核、尾状核、苍白球内部 (GPi) 和丘脑底核 (STN) 中的多个神经元群形成突触。这个复杂的网络形成了从黑质到参与运动的回路(即基底神经节)的传入连接。在基底神经节中,DA 在控制运动和学习新的运动技能方面发挥着关键作用。[ 33 ]
禁忌
患有心脏或循环系统疾病的患者禁用静脉注射多巴胺。这些疾病可能包括室性心律失常和心动过速、血管阻塞、低血氧、血容量减少、酸中毒以及肾上腺功能障碍(例如嗜铬细胞瘤)导致的高血压。对于近期接受单胺氧化酶抑制剂治疗的患者,多巴胺(DA)的初始剂量应为分次剂量(常规剂量的十分之一),并应密切监测后续疗效。用于治疗高血压的药物,例如β-和α-肾上腺素能受体抑制剂,会抵消多巴胺的治疗作用。氟哌啶醇也会阻断多巴胺的全身作用。据报道,抗惊厥药苯妥英钠与多巴胺合用会导致低血压并降低心率。另一方面,三环类抗抑郁药会增强多巴胺的反应,类似于环丙烷和卤代烷等麻醉药。与催产素结合使用 DA 可导致慢性高血压,还可引发脑血管意外。[ 34 ]
儲存條件
置于避光处。
特別說明
有必要监测血压和尿流——还建议监测更复杂的血流动力学参数,例如心输出量,包括心律和肺楔压。值得注意的是,穿透血脑屏障的多巴胺激动剂和类似物会与运动、执行和边缘功能相关的神经回路相互作用,包括与成瘾相关的奖励系统、冲动控制机制和觉醒。因此,停止 DA 治疗会导致一种称为多巴胺激动剂戒断综合征的疾病。这种疾病的症状多种多样,包括焦虑、抑郁、惊恐发作、疲劳、低血压、恶心、易怒甚至自杀意念。[ 43 ] 因此,建议患者逐渐停用这些中枢作用的 DA 激动剂。
保質期
保质期为2年。
多巴胺缺乏
大量研究探讨了多巴胺在运动和感觉运动功能中的作用。因此,在没有药物干预或基因治疗的情况下,多巴胺能末梢的多巴胺缺乏,以及由此产生的多巴胺(DA)耗竭,会导致许多上述功能出现缺陷。[ 44 ]
多巴胺过量
在这种情况下,我们需要用一个例子来解释这种现象。假设一个人开始节食,决心完成他开始的计划。但突然一个美味的蛋糕送到他手上,一切都结束了。于是,这个人就完全控制不住自己了。他需要一剂“快乐激素”,而正是这种甜蜜的喜悦“引发”了这种快乐。所以,他吃了一块蛋糕,然后又吃了第二块,根本停不下来。于是,多巴胺过量就出现了。这没什么可怕的,但一个人很难停下来。
最终,沉迷于生活中的又一个“甜蜜点”,根本无法控制自己。一个人再也无法控制自己。他会继续做同样的事情,最终导致发胖或健康状况恶化。一切都取决于这种快乐激素究竟扮演着怎样的角色。
多巴胺会影响意识活动的诸多方面。有必要降低其水平,避免其过量。但这也可能“危险”,因为降低冲动性可能会损害其他同样重要的功能。
多巴胺再摄取抑制剂
多巴胺再摄取抑制剂 (DRI) 是一类通过阻断多巴胺转运体 (DAT) 的作用来抑制单胺类神经递质多巴胺再摄取的药物。当未被突触后神经元吸收的细胞外多巴胺被阻止重新进入突触前神经元时,就会实现再摄取抑制。这会导致细胞外多巴胺浓度升高,并增加多巴胺能神经传递。[ 48 ]
多巴胺再摄取抑制剂因其精神兴奋剂作用而用于治疗注意力缺陷多动障碍 (ADHD) 和发作性睡病,因其食欲抑制作用而用于治疗肥胖症和暴食症。它们有时被用作治疗情绪障碍的抗抑郁药,但由于强效 DRI 具有很高的滥用可能性且法律限制其使用,因此它们作为抗抑郁药的使用受到限制。当多巴胺能神经传递增加时,多巴胺再摄取不足和细胞外多巴胺水平升高与成瘾行为易感性增加有关。多巴胺能通路被认为在奖励中心有效。许多 DRI,例如可卡因,都是滥用药物,因为大脑中突触多巴胺浓度升高会产生奖励效应。
以下药物具有DRI活性,并且由于其特性而曾或正在临床上使用:阿米普汀、右哌甲酯、双苯吲哚、芬坎法明、利非他明、左苯甲酮、美沙明、美索卡、哌甲酯、诺米芬辛、哌普拉醇、普罗林坦和吡咯戊酮。以下药物目前或曾经在临床上使用,且仅具有较弱的DRI活性,这些活性可能具有或不具有临床意义:阿屈非尼、阿莫达非尼、布丙酮、马吲哚、莫达非尼、奈法唑酮、舍曲林和西布曲明。
多巴胺阻滞剂
D1 和 D2 受体拮抗剂药物会损害许多非条件性行为和条件性行为的表达。例如,D1 和 D2 受体拮抗剂会降低运动活性 [ 49 ]、[ 50 ]、[ 51 ] 以及食欲驱动的操作性行为的发生频率。[ 52 ]、[ 53 ]、[ 54 ]、[ 55 ] 然而,行为表达的至少一个方面,即行为动作的持续时间,似乎受到 D2 受体拮抗剂(相对于 D1)相对特异性的调节。
我们之前观察到,全身性 D1 受体阻滞剂会降低条件刺激 (CS) 引发趋近反应的试验比例,而我们在 D2 受体阻滞剂后并未观察到这种效应。[ 56 ] 其他研究也类似地报告称,提示反应表达会因 D1[ 57 ] 受体阻滞而受损,但不会因 D2[ 58 ],[ 59 ] 受体阻滞而受损,尽管有几项研究观察到 D2 拮抗剂会导致提示反应表达受损。[ 60 ],[ 61 ]
多巴胺交换
你知道多巴胺是如何交换的吗?如今,人们正在积极寻找具有多巴胺能效应的药物。由于多巴胺的长期缺乏,受体的功能状态可能会发生各种变化。
长期治疗会导致多巴胺能受体发生不可逆的变化。但这并不能阻止突触前神经元的逐渐退化。因此,研究人员开始寻找能够刺激突触后受体并使其对治疗更敏感的特殊方法。这些方法包括多巴胺能激动剂。但也存在一些担忧。例如,长期使用多巴胺能激动剂可能会导致酪氨酸羟化酶活性被抑制。
 [ 62 ]、[ 63 ]、[ 64 ]、[ 65 ]、[ 66 ]、[ 67 ]
[ 62 ]、[ 63 ]、[ 64 ]、[ 65 ]、[ 66 ]、[ 67 ]
多巴胺的产生
科学家已经证明,任何能带来愉悦的活动都能促进快乐激素的分泌。因此,一个人做什么并不重要,重要的是它能让他感到快乐。当然,活动应该在合理的范围内。如果排除所有快乐,多巴胺水平就会显著下降,人就可能陷入抑郁。
需要了解的是,多巴胺被认为是一种药物成瘾。因为爱吃蛋糕的人会不断地吃蛋糕来改善心情。这会导致其他问题,例如健康状况不佳、体重超标等等。如果剥夺了这种“快乐”,就会出现抑郁,情绪也会恶化。最终,这是一个恶性循环。因此,你需要选择更有益的活动。
触发多巴胺“分泌”最简单、最愉悦的方式就是规律的性生活。但前提是这种活动真的能带来愉悦感。
 [ 68 ], [ 69 ], [ 70 ], [ 71 ]
[ 68 ], [ 69 ], [ 70 ], [ 71 ]
多巴胺与精神分裂症
多巴胺假说的起源有两条证据。首先,临床研究证实,多巴胺能激动剂和兴奋剂可诱发健康个体的精神病,并加重精神分裂症患者的精神病症状。[ 72 ] 其次,研究发现抗精神病药物会影响多巴胺系统。[ 73 ] 后来,抗精神病药物的疗效与其对多巴胺D2受体的亲和力相关,从而将分子作用与临床表型联系起来。[ 74 ]
尸检研究首次提供了脑内多巴胺能功能障碍及其解剖位置的直接证据。研究显示,精神分裂症患者纹状体中的多巴胺及其代谢物和受体水平升高。[ 75 ],[ 76 ] 然而,这些研究涉及接受抗精神病药物治疗的患者。因此,尚不清楚这种功能障碍是否与疾病的发作或终末期有关,或者是否与抗精神病药物的作用有关。
 [ 77 ]、[ 78 ]、[ 79 ]、[ 80 ]、[ 81 ]、[ 82 ]、[ 83 ]、[ 84 ]、[ 85 ]、[ 86 ]
[ 77 ]、[ 78 ]、[ 79 ]、[ 80 ]、[ 81 ]、[ 82 ]、[ 83 ]、[ 84 ]、[ 85 ]、[ 86 ]
多巴胺和多巴胺
所以,这些物质本身并没有什么区别。因为它们本质上是一样的。这种物质在体内产生,并发挥神经递质的作用。简而言之,它帮助脑细胞传递某些信息。通俗地说,这种物质被称为“快乐激素”。
多巴胺的产生会带来活力四射、心情愉悦、精力充沛,以及记忆力和注意力的提升。事实上,它有很多好处。值得注意的是,这种物质可以通过生活中的“甜味剂”来产生。这些甜味剂可以是食物,也可以是体育锻炼。简而言之,任何让人快乐的事情都会刺激这种激素的产生。因此,你需要更频繁地去做那些能带来完全满足感的事情。
多巴胺和多巴胺是同一种物质,发挥着相同的功能。保持快乐激素的水平很重要,这样生活才会更加充实。
酒精对多巴胺系统的影响
向伏隔核 (NAc) 壳层传递信息的多巴胺能神经元对酒精极其敏感。例如,在大鼠研究中,以每公斤体重 2 至 4 毫克的剂量注入血液,可增加 NAc 壳层中的多巴胺释放,并支持长期自我饮酒。[ 89 ] 大鼠口服酒精也会刺激 NAc 壳层中的多巴胺释放。[ 90 ] 然而,与直接向血液中注射酒精相比,这种给药途径需要更高剂量的酒精才能达到相同的效果。[ 91 ]
酒精刺激内源性阿片肽(NAc)释放多巴胺可能需要另一类神经调节剂——内源性阿片肽——的活性。这一假设得到了以下观察结果的支持:抑制内源性阿片肽作用的化学物质(即阿片肽拮抗剂)可以阻止酒精对多巴胺释放的影响。阿片肽拮抗剂主要作用于大脑中投射到NAc的多巴胺能神经元的起源区域。这些观察结果表明,酒精刺激内源性阿片肽活性,间接导致多巴胺能神经元的激活。阿片肽拮抗剂可能干扰这一过程,从而减少多巴胺的释放。
酒精作为强化剂的作用:多巴胺的作用
尽管许多研究试图通过操纵多巴胺信号来阐明多巴胺在酒精强化中的作用,但这些研究并不能得出任何确切的结论。[ 92 ] 然而,将酒精的作用与食物等常见强化物的作用进行比较,可以为多巴胺在介导酒精强化中的作用提供一些线索。
例如,美味的食物会通过提供某些感官刺激(例如,味觉或风味)来激活NAc壳层中的多巴胺能信号。口服酒精同样会激活味觉受体,从而增加NAc中的多巴胺释放。然而,与食物不同,酒精一旦到达大脑,就会直接改变多巴胺能神经元的功能。因此,口服酒精既通过其味觉特性(即作为常规强化剂)影响NAc中的多巴胺释放,也通过其对大脑的直接作用(即作为药物强化剂)影响NAc中的多巴胺释放。与此假设一致,NAc中出现了两个多巴胺释放峰。第一个峰来自与酒精相关的味觉刺激;第二个峰来自酒精对大脑的影响。因此,酒精诱导的多巴胺能信号直接激活可以增强酒精相关味觉刺激的激励特性。由于这种机制,与酒精相关的味觉刺激获得了强大的激励特性(即,它们成为动机刺激,促使饮酒者寻求更多酒精)。同样,与酒精相关的食欲刺激(例如,外部刺激,例如特定品牌酒精饮料的出现或酒吧的出现)也获得了激励特性,并促进酒精的寻求和消费。通过这些复杂的机制,酒精诱导的多巴胺释放激活了促进酒精消费的二级强化回路。
多巴胺在酒精成瘾发展中的作用
NAc壳层中的多巴胺释放可能促使酒精依赖的形成。酒精心理依赖的形成是因为与酒精相关的刺激物获得了过度的激励特性,从而引发了饮酒的强烈欲望(即渴求)。由于这种强烈的渴求,正常的强化刺激(例如食物、性、家庭、工作或爱好)失去了意义,对饮酒者的行为的影响也随之减弱。
酒精相关线索所导致的异常意义,可能源于酒精诱导的NAc多巴胺能信号上调的适应不良性。如前所述,正常强化物(例如食物)会诱导NAc壳层多巴胺释放增强,从而迅速形成习惯,而反复呈现相关刺激不再引发多巴胺释放。相反,反复饮酒后不会产生习惯。由于NAc壳层对酒精的反应持续释放多巴胺,酒精相关刺激会获得异常的情绪和动机意义,导致饮酒者对其行为产生过度控制。这种过度控制正是成瘾的核心。
 [ 93 ], [ 94 ], [ 95 ], [ 96 ], [ 97 ]
[ 93 ], [ 94 ], [ 95 ], [ 96 ], [ 97 ]
吸烟和多巴胺
烟草使用障碍受多种环境和遗传因素的影响。环境因素涵盖广泛的文化、社会和经济方面。遗传因素可分为两大类:与尼古丁代谢途径相关的基因,该途径指示某人将尼古丁代谢为可替宁的速度;以及与奖赏级联理论相关的基因,该理论指示吸烟时体验到的快感程度。影响尼古丁代谢的最重要基因是细胞色素 P450 CYP2A6 和 CYP2B6。影响奖赏级联理论的基因包括血清素、阿片类药物、γ-氨基丁酸 (GABA) 和多巴胺的复杂网络。[ 98 ]
请阅读本文有关多巴胺候选基因和吸烟的研究。
如何增加多巴胺?
其实这个过程并不复杂,你只需要尽量把那些能带来快乐的活动纳入你的日常计划即可。
但这还不是全部。因此,建议每天吃香蕉。香蕉含有一种类似多巴胺的物质。香蕉上的小棕色斑点含有大量这种有用的“物质”。饮食中应该富含抗氧化剂。抗氧化剂属于能自行提高多巴胺水平的自由基。这类食物包括红豆、蔓越莓、朝鲜蓟、草莓、李子和蓝莓。
戒掉脱咖啡因咖啡、减少糖分摄入以及减少酒精饮料的摄入是有益的。建议每天吃一把杏仁,葵花籽也是不错的选择。芝麻也是不错的选择,它可以作为任何沙拉和新鲜蔬菜三明治的绝佳配料。
食物中的多巴胺
多巴胺在人体中发挥着重要作用,有助于协调身体运动、动机和奖赏机制。关于多巴胺产品含量的信息非常有限,这可能是由于缺乏临床研究。芭蕉属的果实,例如香蕉和梧桐树,以及美洲鳄梨(M. Persea americana,即鳄梨)含有高浓度的多巴胺。[ 102 ] 尤其是在香蕉皮(700 μg/g)、香蕉果肉(8 μg/g)和鳄梨(4-5 μg/g)中检测到了多巴胺。在植物中,多巴胺起着保护作用,并参与生殖器官发生、离子通透性、抗氧化活性[ 103 ]以及生物碱的形成。 [ 104 ] 有趣的是,黧豆(Mucuna pruriens L.,即藜豆)的叶子已被证明含有多巴胺,[ 105 ] 因此可能参与了种子衍生产品众所周知的抗帕金森病作用。[ 106 ] 在柑橘(Citrus sinensis L.,即橙子)、苹果(Malus sylvestris L.,即木苹果)、番茄、茄子、菠菜、豌豆和豆类中检测到了低水平的多巴胺。据报道,饮用脱脂牛奶后会出现发作性运动障碍(即左右摇头)。同一作者将这些影响归因于乳制品中高含量的L-酪氨酸。[ 107 ] 然而,不能排除可能存在多巴胺相互作用,但文献数据不足。
注意!
為了簡化對信息的理解,本指令使用了藥物 "多巴胺",並根據藥物的醫療用途官方說明。 使用前請閱讀直接用於藥物的註釋。
描述僅供參考,不適用於自我修復指導。 這種藥物的需求,治療方案的目的,藥物的方法和劑量僅由主治醫師確定。 自我藥療對你的健康有危害。


