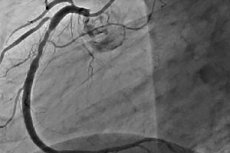
经腔内球囊冠状动脉成形术(TBCA)后的再狭窄
经皮冠状动脉血管造影 (TBCA) 术后,术后前 6 个月内再狭窄的发生率为 30-40%。其主要机制是血管局部负性重塑,本质上是动脉管腔的弹性塌陷,在术中被球囊扩张。局部血栓形成和新生内膜生长也起着相对作用。TBCA 术后再狭窄的危险因素包括临床(2 型糖尿病、急性冠状动脉综合征 (ACS)、再狭窄病史)、血管造影(左前降支 (LAD) 病变、血管直径小、慢性完全闭塞 (CTO)、长病变、静脉旁路移植血管退化)和手术(残余狭窄面积大、球囊扩张后血管直径增加不大)等。如果出现再狭窄,通常需要再次干预。在再狭窄部位再次进行 TBCA 的成功率与首次手术相当。然而,每次后续 TBCA 治疗再狭窄,复发性再狭窄的风险都会显著增加。第三次尝试后,再狭窄发生率达到50-53%。此外,每次重复TBCA后,再狭窄的发生率都比第一次更明显。第二次TBCA后再狭窄的危险因素包括:首次再狭窄出现较早(术后60-90天)、左前降支(LAD)损伤、多支血管损伤、2型糖尿病、动脉高血压、不稳定型心绞痛以及首次手术期间多次球囊扩张。鉴于再狭窄的高发生率及其发展机制,冠状动脉支架被引入临床实践,理论上支架应该可以消除TBCA后的负性血管重塑。
第一批证明支架疗效的研究是 1993 年发表的 STRESS 和 BENESTENT 研究。BENESTENT 纳入了 516 名新诊断为冠状动脉直径大于 3 毫米狭窄的患者,将他们随机分为两组:传统 TBCA(n = 257)和支架置入型 TBCA(n = 259)。3 年后,血管造影期间的再狭窄发生率在传统 TBCA 组为 32%,在支架置入组为 22%。再狭窄发生率相对降低了 31%(p < 0.01)。支架置入组再次心肌血运重建的需求也较低(10% vs. 传统 TBCA 组为 20.6%;p < 0.01),这与支架置入组心绞痛复发率较低有关。
根据 STRESS 研究 (n = 407),支架组 (n ~ 205) 的再狭窄发生率也低于传统 PTCA 组 (n = 202) — 31.6% vs. 42.1% (p < 0.01)。REST 研究表明,在 PTCA 部位出现再狭窄时使用支架比传统血管成形术更有优势,该研究将 383 名再狭窄患者随机分配接受支架植入术或再次经皮腔内冠状动脉成形术。支架组经血管造影检测到的再次再狭窄发生率低 18% (18% vs. 5.32%;p < 0.03)。接受支架植入术的患者中,再次心肌血运重建(临床上显著再狭窄的指标)的需要率也显著降低 (10% vs. 27%;p < 0.001)。因此,不仅在原生动脉中使用支架植入术可获得更好的效果,而且在 TBCA 后出现的再狭窄干预情况下也同样如此。
裸支架植入后再狭窄(BSI)
尽管与TBCA相比,未覆盖的冠状动脉支架已将再狭窄发生率降低了30-40%,但即使在支架置入后,仍有17-32%的患者会出现支架内再狭窄,需要再次进行血运重建。支架内狭窄(ISS)的发生机制与TBCA不同。支架置入后,再狭窄的主要原因是新内膜形成,而非像TBCA那样在支架置入部位几乎不存在负性重塑。新内膜是由平滑肌细胞迁移和增殖形成的,这些细胞产生细胞外基质,这些基质与细胞共同构成新内膜。此外,血栓在支架置入部位的持续存在对于糖尿病患者也至关重要。
支架内狭窄 (ISS) 的主要分类是 Mehrаn 提出的分类,根据病变范围和严重程度分为四型:I 型 ISS - 局部性(长度 < 10 毫米),II 型 - 弥漫性(长度 > 10 毫米),III 型 - 增生性(长度 > 10 毫米且延伸至支架外),IV 型 - ISS 导致闭塞。I 型 ISS 根据其在支架内的位置又分为以下亚型:1a - 位于弯曲处或支架之间,1b - 边缘性,1c - 位于支架内,1d - 多灶性。
发生静脉旁路再狭窄 (VRS) 的风险因素包括静脉旁路移植术干预、慢性闭塞、开口病变、血管直径较小、存在残留狭窄、VRS 支架置入术、术后血管直径较小、左前降支 (LAD) 病变、支架长度较长、糖尿病、在单个病变处植入多个支架。有迹象表明遗传因素会影响该病,尤其是糖蛋白 IIIa 基因的多态性和亚甲基四氢叶酸还原酶基因(编码白细胞介素-1 的基因)的突变。在发生边缘性支架再狭窄的情况下,主要风险因素是支架置入段的明显动脉粥样硬化病变。
血管再狭窄主要发生在经皮冠状动脉介入治疗(PTCA)后的前6-8个月内。大多数患者大约在同一时间出现临床症状。血管再狭窄综合征(VRS)通常表现为复发性心绞痛。不稳定性心绞痛较少见(占11-41%)。1-6%的患者会发展为AMI。因此,支架置入后1-6个月内心绞痛最常见的原因是VRS,通常需要再次进行血运重建。治疗VRS的方法有多种。可以进行常规的TBCA,这会导致支架进一步扩张(占血管直径最终增加的56%),并将新生内膜推过支架细胞(占血管直径最终增加的44%)。然而,大多数情况下,在介入部位会观察到残留的血管再狭窄(平均18%)。此外,11% 的 TBCA 术后患者需要再次血运重建,尤其对于多支血管病变、左心室射血分数 (LVEF) 低、接受静脉旁路移植术或首次发生 VRS 的患者。TBCA 术后再次发生 VRS 的风险也取决于病变类型,范围从局部再狭窄的 10% 到支架内闭塞的 80% 不等。与单纯 TBCA 相比,在 VRS 部位植入 LES 并不能降低其复发风险。
治疗血管内支架置入综合征 (VRS) 的第二种方法是近距离放射治疗,即将放射源引入冠状动脉管腔,防止平滑肌细胞增生,从而降低再狭窄风险。然而,由于设备成本高昂、操作技术复杂以及晚期支架内血栓形成 (LT) 发生率较高,近距离放射治疗几乎完全无法在临床上使用。
药物洗脱支架的引入是VRS治疗的革命性时刻。与自身动脉中的LES相比,它们可将VRS风险降低70-80%。TAXUS III患者注册研究获得了关于DES对已发生VRS患者的有效性的首批数据,其中,当对此类患者使用SPG1时,6个月后VRS复发率仅为16%,低于前面提到的TBCA研究的复发率。TRUE注册研究纳入了因LES再狭窄而植入SES的患者,结果显示,9个月后,不到5%的患者需要再次血运重建,这些患者主要患有糖尿病和ACS。TROPICAL研究比较了在再狭窄部位植入DES后患者的再次再狭窄率,并与GAMMA I和GAMMA II研究的数据进行了比较,后两项研究均采用近距离放射治疗作为治疗方法。 6 个月后,SPS 组复发性血管重建的发生率显著降低(9.7% vs 40.3%;p < 0.0001)。值得注意的是,SPS 组支架内血栓形成和心肌梗死的发生率也较低(TS 0.6% vs 3.9%;p = 0.08;MI - 1.8% vs 9.4%;p = 0.004)。随机 SISR 研究证实了 SPS 优于近距离放射治疗,其中 384 名 NSC 中出现 VRS 的患者被随机分配到近距离放射治疗组或 SPS 植入组。9 个月后,近距离放射治疗后再次血运重建的需求 (19.2%) 高于 SPS 植入组 (8.5%),这反映了血管重建再狭窄的复发率更高。 3年后,SPS在减少因支架内再狭窄复发而需要再次血运重建方面的优势依然存在(19% vs 28.4%)。两组间血栓形成发生率无显著差异。
下食管 (LES) 患者在植入 SPS 后发生复发性肾小管狭窄 (VRS) 的主要因素包括血管直径较小(< 2.5 毫米)、弥漫性再狭窄以及存在需要血液透析的慢性肾衰竭。在随机研究 TAXUS V ISR 中,SPS 也显示出治疗 VRS 的高效性,与近距离放射治疗相比,其复发性再狭窄发生率降低了 54%。
还进行了比较 TBCA 对 VRS 和 DES 植入疗效的随机试验。在随机 RIBS-II 试验中,9 个月后,DES 植入后的再次再狭窄发生率比 TBCA 后低 72%,将再次血运重建的需求从 30% 降至 11%。ISAR DESIRE 试验比较了 TBCA 对 VRS 与 SPP 或 SPS 植入的疗效。6 个月后,结果表明,两种 DES 在预防再次再狭窄方面均比 TBCA 更有效(TBCA 组发生率为 44.6%,SPS 组为 14.3%,SPS 组为 21.7%),这减少了再次血运重建的需求。在 SPP 和 SPS 的直接比较中发现,SPS 比 SPP 更有效地减少了再次血运重建的需求(8% vs. 19%)。因此,与 TBCA 和近距离放射治疗相比,DES 植入可降低复发性 LES VRS 的发生率,从而减少重复 PCI 的数量,因此 DES 植入成为此类患者的首选手术。
药物洗脱支架(DES)植入后的再狭窄
尽管与 LES 相比,使用 DES 时支架内狭窄的发生率降低了 70-80%,但并不能完全排除这种支架置入术的医源性后果的发生。其总体发生率平均仍然低于 10%。除了再狭窄发生率的数量下降之外,他们还显著改变了发生的再狭窄类型。因此,植入 DES 后,再狭窄通常是局灶性的。临床上,与 LES 的情况一样,它最常表现为稳定型心绞痛复发(77%),较少见(8%)是无症状的。5% 的病例表现为不稳定型心绞痛,10% 的病例其首发症状是非 Q 波心肌梗死。2 型糖尿病、小血管直径和病变范围是 DES 再狭窄发展的主要因素。目前尚无针对此类患者管理的明确建议。替代方案包括重新植入药物洗脱支架(同类型或不同类型)、经皮冠状动脉造影 (TBCA) 或近距离放射治疗。第二次植入药物洗脱支架 (DES) 的平均再狭窄率为 24%,无论植入同类型还是不同类型 DES,该比例均相同。



 [
[